单颗粒ICP-MS应用:西红柿吸收金纳米颗粒
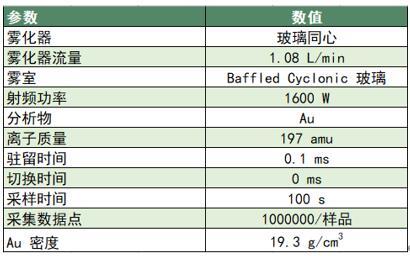
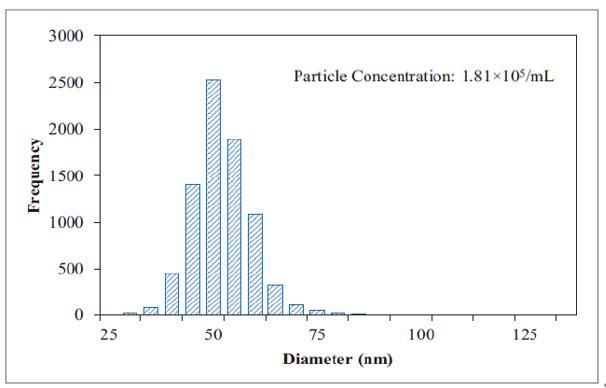
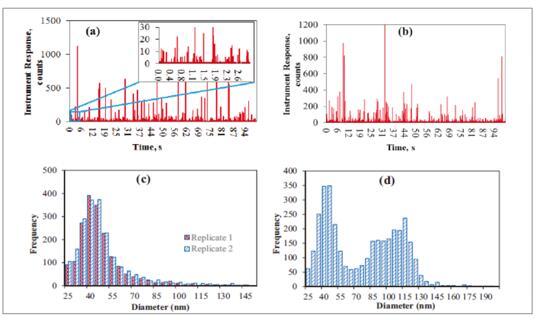
实验与分析
展源
何发
相关文章
-

单颗粒ICP-MS测定复杂基质中的纳米颗粒
2021-12-03
-

单颗粒ICP-MS应用:通用池技术消除铁纳米颗粒质谱干扰
2021-03-05
-

ICP-MS大家谈
2020-05-27
-

QC, IQC, IPQC, QA,到底是什么鬼?
2020-05-27
-

AAS法分析茶叶中的铅,镉,砷
2020-05-27
-

ICP-MS实用指南
2021-01-07
-

【收藏】180个ICP-MS常见问题与答案
2024-05-23
-

国产ICP-MS技术进展
2023-01-17
-

ICP-MS升级环境实验室
2020-05-27

加载更多