从焰色反应到原子发射光谱分析
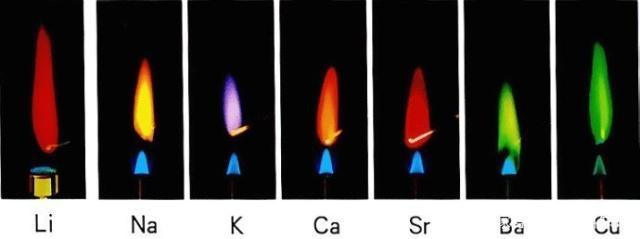
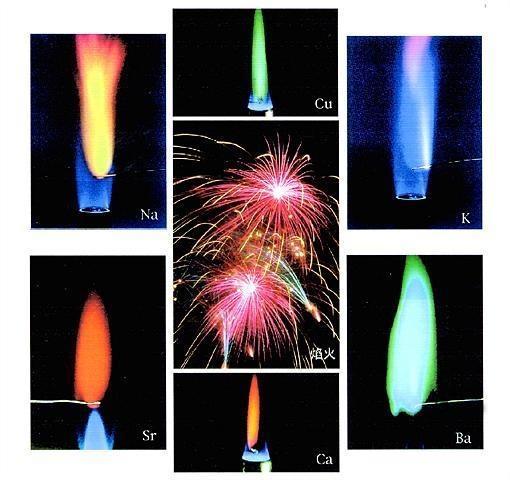
几百年前,化学家们就企图凭着物质在火焰中发出的颜色来研究物质的组成。直到1854年,德国化学家本生发明了本生灯,才有可能在较高的温度和较少的于扰下系统地研究这个问题。本生用一根白金丝分别把各种各样的物质送进本生灯的火焰中,他惊喜地发现各种金属的盐类在高温下都能发出自己特有的彩色光。钠是黄色,钾是紫色,钙是砖红色,钡是绿色……这种特异的现象被叫做焰色反应。
但是,当本生进一步着手利用焰色反应来判断物质中所含的元素成分时,他发现这并不是一种非常容易的事。除了钠等极少数金属元素能直接通过观察得出外,大部分金属元素在火焰中的颜色都是相互覆盖的,就是用各种颜色的滤色片也极难把它们辨出来。例如:锶蒸气和锂蒸气都能将灯焰染成红色,两者根本无法用肉眼辨别。
物理学家基尔霍夫在一次散步中向隋入困境的本生建议,是否可以利用物理的研究成果,设法观察火焰的光谱而不是直接观察火焰的本身。于是,他们制作了一部简单的分光镜,在镜筒的一头开了条狭缝作为平行光管,使通过平行光管的光线落到三棱镜上,三棱镜进一步把从狭缝里射来的光线向一旁折射,形成了光谱。化学家和物理学家的相互合作立即得到了惊人的发现:钠盐的光谱在全黑的背景上出现了两条明亮的黄线,而且这两条黄线永远是出现在同一位置上,所有的钾盐都产生了一条紫线和一条红线,两条谱线当中的光谱差不多是连成一片的;所有的锶盐的光谱上都有条明亮的蓝线和几条暗红线。
总之,每一种元素都有它特有的谱线,在三棱镜的折射下,都出现在它们各自固定的位置上。这样一来,要从被检物质里寻找元素的组成,就可以根据各种元素的特征谱线来确定这种元素的存在。下本现代的原子发射光谱分析就是在这个基础上发展起来的。随着对原子光谱更深入的研究,人们发现物质中不同的原子之所以会产生不同的光谱,是由于不同的原子会产生不司的能级的跃迁。当把含有不同原子的试样放入光源中,试样首先蒸发变成气态原子,并吸收光源的能量,使外层电子激发至高能态,面处于商能(激发)状态的原子不稳定,又跃迁回基态或低能态,便产生不同波长的辐射。
现在的光源已不再用本生灯了,而是用能给予更高能量,于扰更小的直流或交流的电弧发生器高压火花器和激光显微光源,用摄谱仪代替三棱镜进行分光,按波长的顺序记录在感光板上。随着各种先进技术的广泛应用,8年代的原子发射光谱分析,已应用更先进的光谱仪配合电子计算机进行自动进样及数据处理,不但可以确定物质的元素组成,而且可以根据各特征谱线强度,精确地确定各种元素的含量,在几分钟甚至几十秒内就能完成100多年前需要几个月甚至几年才能完成的分析工作。
实验与分析
展源
何发
- 金属材料直读光谱成分检测
- 没有了
相关文章
-
红外光谱分析,你了解多少?
2021-01-11
-

AAS法分析茶叶中的铅,镉,砷
2020-05-27
-

QC, IQC, IPQC, QA,到底是什么鬼?
2020-05-27
-

影响火焰原子吸收光谱仪灵敏度的因素?
2023-02-09
-

影响火焰原子吸收光谱仪灵敏度的因素有那些
2023-02-08
-
(7).jpg?x-oss-process=image/resize,m_pad,w_80,h_60,color_eeeeee)
什么是焰色反应?
2020-05-27
-
检测有机氯类农药,气相色谱法检测法
2021-01-12
-

原子发射光谱的5大光源特点及原理
2020-05-27
-
原子发射光谱实验-氩气源及其使用
2020-05-27

加载更多